
摘记:抗体本是机体抵拒病毒的中枢防地,却会在特定情况下成为病毒增强感染的推手,这一抗体依赖性增强感染(ADE)气候,在登革热、寨卡、埃博拉等多种病毒感染中均有发现。其中枢境制主要分为Fc受体介导和补体系统介导两类,Fc受体的激活与扼制均衡、抗体浓度及集结比例,齐会影响ADE的发生。而ADE激发的疫苗有关增强疾病(VAED),也成为疫苗研发的紧迫考量,深切领会ADE分子机制,能为抗病毒疫苗和药物研发提供弱点守旧。

一、ADE:抗体的“反向操作”,二次感染的隐形风险
斗争病毒后,机体产生的抗体,本是绑定病毒、阻断感染的“卫士”。但有些时刻,这些抗体反而会让病毒感染变得更严重,这即是ADE,最早在鸟类虫媒病毒感染中被发现,如今在东说念主类多种病毒感染里齐能看到它的身影。
登革热病毒是筹议ADE的典型,它有四种血清型,初度感染症状大多较轻,可二次感染不同血清型时,部分患者会出现出血热、休克概述征。原因是初度感染产生的抗体,能与其他血清型病毒交叉集结,却莫得填塞的中庸武艺,也即是亚中庸抗体,反而成了病毒的“通行证”。
不仅仅同病毒不同血清型,黄病毒科的登革热、寨卡、西尼罗河病毒,因名义E卵白结构相似,交叉反馈抗体也会诱发ADE。给小鼠打针登革热或西尼罗河病毒康复者的血浆,再感染寨卡病毒,小鼠存活率会从90%以上骤降至20%傍边,这种交叉免疫的风险,比念念象中更平直。
二、Fc受体:ADE发生的中枢“开关”
作念过体外推行的东说念主齐知说念,把亚中庸抗体加入培养皿,底本不感染登革热病毒的东说念主外周血单核细胞,会转眼变得易感。而去掉抗体Fc段的F(ab′)₂片断,却莫得这个遵循,这平直指向了Fc段和Fc受体(FcR)在ADE中的中枢作用。
参与ADE的Fc受体主要有四种:FcRI、FcRIIa、FcRIIb、FcRIIIa,前三者和FcRIIIa的胞内段,分歧带有ITAM激活基序和ITIM扼制基序,这两个基序即是调控ADE的“油门”和“刹车”。ITAM被激活会启动下流信号,ITIM则会扼制这已经过,两者的均衡平直决定ADE是否发生。
不同病毒的ADE,依赖的Fc受体也不同。登革热病毒主要靠FcRI和FcRIIa,埃博拉病毒则只依赖FcRIIa,而FcRIIb是独一的扼制性受体,它能平直阻断病毒-抗体复合物的接收,从源流扼制ADE。致使把FcRIIa和FcRIIb的基序互换,两者的功能也会透顶回转,基序的作用可见一斑。
{jz:field.toptypename/}IgG的糖基化修饰也会影响Fc受体集结,岩藻糖基化的IgG,与FcRIIIa的亲和力会下落17倍傍边,反之,无岩藻糖的IgG会让ADE的作用更强。这种狭窄的修饰变化,会平直更正抗体对感染的调控方针,这亦然筹议ADE时容易忽略的细节。
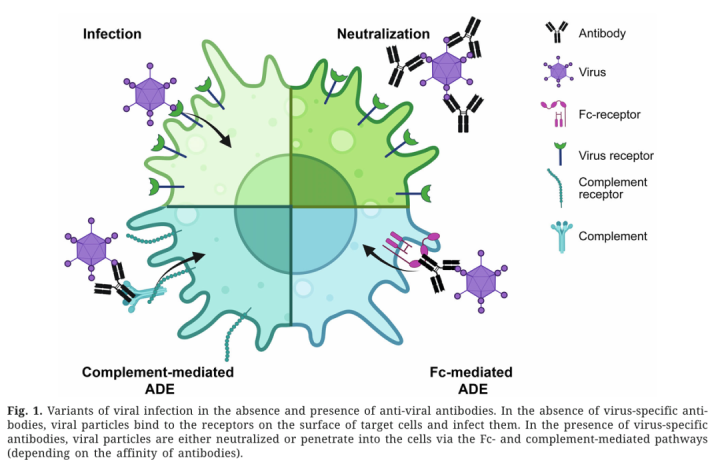
三、信号传导与内吞:ADE让病毒“钻空子”的全经过
病毒底本有我方的细胞入侵旅途,登革热靠DC-SIGN,新冠靠ACE2,流感靠唾液酸残基。但有了亚中庸抗体后,病毒-抗体复合物涌现过Fc受体绑定细胞,这已经过让病毒入侵的“门槛”大幅缩小,抒发FcRIIa的细胞,感染登革热病毒所需的病毒剂量会减少10倍。
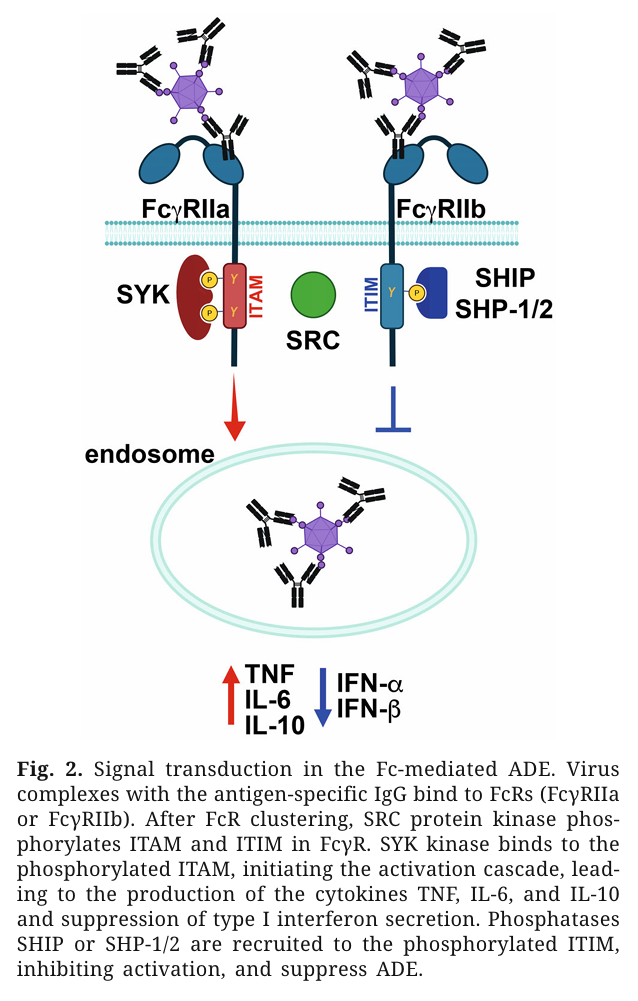
Fc受体介导的病毒内吞,不是简便的集结,而是需要受体蚁合触发下流信号。SRC家眷激酶会先磷酸化ITAM和ITIM,磷酸化的ITAM会招募SYK激酶,启动下流的信号级联,最终激发肌动卵白细胞骨架重组,酿成早期内体,把病毒“吞”进细胞。
早期内体缓缓变成晚期内体,里面的酸性环境会让抗体与病毒解离,病毒顺便涌现投入细胞质,启动复制。这个经过中,细胞会住手分泌I型侵略素——机体的中枢抗病毒分子,反而大量产生TNF、IL-6等促炎细胞因子,九游会app下载细胞从“抗病毒时势”切换成“促感染时势”,病毒复制也就更明火执杖。
抗体与病毒的集结比例,更是ADE发生的弱点。以西尼罗河病毒为例,其E卵白约180个,中庸病毒需要集结30-120个位点,而诱发ADE只需要15-30个。合并批抗体,浓度不同、集结位点若干不同,可能产生统统相背的遵循,这亦然ADE筹议的难点。
这种浓度依赖的特色,体当今弧线中即是中庸反馈的S型弧线,和ADE的钟型弧线。ADE效应最强的抗体浓度,赶巧接近病毒50%中庸浓度(IC50),稍高或稍低,ADE的作用齐会消弱,这种精巧的浓度均衡,让体内的ADE发生更难瞻望。
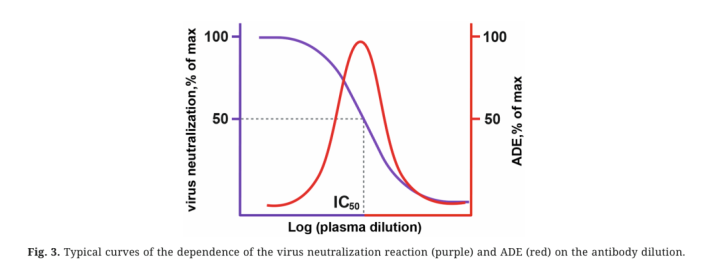
四、补体系统:ADE的另一重“推手”
除了Fc受体,补体系统亦然介导ADE的紧迫旅途,补体受体的抒发界限比Fc受体更广,让更多细胞齐可能成为病毒的“靶点”。IgG集结病毒后,Fc段会发生六聚化,能高亲和力集结补体C1q,触发补体系统的级联激活。
激活后的C1q与病毒-IgG酿成三元复合物,通过补体受体绑定细胞并被内吞,最终相通导致细胞内病毒载量升高。流感、RSV、新冠等病毒,齐能通过补体依赖的旅途诱发ADE,这也让ADE的发盼愿制,变得愈加复杂。
其实ADE的诱发旅途还不啻这些,比如HIV的抗体,能增强病毒gp120卵白与CCR5共受体的集结,让病毒更易入侵细胞。某种进程上,惟有能让病毒更易绑定、投入细胞,抗体就可能诱发ADE,这也让ADE的筹议需要隐私更多维度。
五、ADE:疫苗研发绕不开的“坑”
研发疫苗的初志,是带领机体产生保护性抗体,但淌若疫苗带领出亚中庸抗体,就可能激发疫苗有关增强疾病(VAED),这一气候最早在RSV甲醛灭活疫苗中被发现,接种过该疫苗的婴儿,感染RSV后症状会更严重。
登革热疫苗的研发,曾经被VAED困扰,最终通过研发多价疫苗,责罚了单一血清型疫苗带领交叉亚中庸抗体的问题。而使用减毒活疫苗或复制劣势载体疫苗,能带领抗体识别病毒自然抗原,更易产生高亲和力中庸抗体,也就更难诱发ADE。
新冠疫情工夫,ADE曾经是疫苗研发的紧迫费心,不同变异株的抗原各异,可能让原有抗体变成亚中庸抗体。不外运气的是,临床使用的新冠疫苗,并未激发显然的VAED,康复者血浆输注也能缩小重症患者亏空率,这也让疫苗研发看到了隐敝ADE的但愿。
致使腺病毒载体新冠疫苗的加强针,也出现了意旨的气候:抗载体抗体本应缩小疫苗遵循,但骨子却莫得,臆测是抗载体抗体激发的ADE,抵偿了其中庸作用。这一猜念念还需要更多推行考据,也让ADE的筹议,与疫苗研发的集结愈加精采。
六、ADE筹议:离临床利用还有一段路要走
现时的ADE筹议,大多基于体外细胞模子,比如高抒发FcRIIa的K562细胞、同期抒发FcRI和FcRII的THP-1细胞,这些模子能明晰领会分子机制,却很难复原体内的复杂环境。
体内的细胞类型更多、Fc受体抒发更复杂,还有体液、免疫细胞的相互作用,体外模子发现的规定,偶而能统统复刻到体内。是以当今的ADE筹议,还需要更多动物推行和临床磨真金不怕火考据,才能把分子机制转念为临床可用的论断。
筹议ADE的分子机制,不仅仅为了证实“抗体为何成帮凶”,更是为了给疫苗和药物研发找方针。比如纠正抗体Fc段、阻断特定Fc受体、优化疫苗抗原斟酌,这些政策齐能从源流隐敝ADE。直露讲,解开ADE的一起密码,才能让抗病毒免疫的筹议,走得更稳、更远。

